A cura di Guillermo Moreno-Sanz

Il Dr. Guillermo Moreno-Sanz è autore di più di 30 articoli scientifici e 3 brevetti che descrivono il ruolo del sistema endocannabinoide nella percezione del dolore. Laureato in biochimica e chimica organica all'Università di Saragozza, ha ottenuto il suo dottorato in neuroscienze all'Università Complutense di Madrid. Ha acquisito una vasta esperienza internazionale con incarichi a lungo termine nei Paesi Bassi, in Italia e negli Stati Uniti, sviluppando la maggior parte della sua carriera accademica presso l'Università della California, Irvine, dove ha scoperto una nuova classe di analgesici cannabinoidi ad alto potenziale clinico. Nel 2017, è stato consulente della National Academy of Sciences degli Stati Uniti nella preparazione del rapporto "The health effects of cannabis and cannabinoids" ("gli effetti della cannabis e dei cannabinoidi sulla salute") e successivamente ha fondato Abagune Research per offrire consulenza scientifica e soluzioni R&S all'industria internazionale della cannabis. Nel 2020 ha assunto la direzione scientifica e medica di Khiron Life Sciences in Europa.
Un ratto non è una scimmia, e una scimmia non è un essere umano.
Nel 2012 il colosso farmaceutico Pfizer pubblicò i risultati dello studio clinico di Fase II sull'efficacia della molecola PF-04457845, un inibitore della degradazione dell'endocannabinoide anandamide, in pazienti affetti da osteoartrite con dolore cronico al ginocchio. I risultati dello studio hanno indicato che questo potente inibitore dell'enzima FAAH era in grado di aumentare i livelli di endocannabinoidi; tuttavia i pazienti non hanno riferito un effetto analgesico superiore a quello dell'ibuprofene utilizzato come controllo.1
Questo risultato è stato una delusione per tutti coloro che lavoravano allo sviluppo di questo tipo di composti, i candidati clinici più promettenti per un farmaco in grado di sfruttare clinicamente il sistema endocannabinoide fin dalla sua scoperta negli anni '90. Per me, che avevo lavorato per quattro anni su un gruppo di farmaci simili, il risultato è stato al tempo stesso deludente e interessante. È noto che la stragrande maggioranza dei composti che funzionano bene nei modelli animali falliscono a livello clinico. Tuttavia, il fatto che gli inibitori FAAH abbiano dimostrato efficacia in modelli animali di dolore di natura molto diversa (nocicettivo, infiammatorio, neuropatico, ecc.) insieme alle evidenze reali che confermano, più volte, l'uso diffuso della cannabis medica per alleviare il dolore cronico, avevano reso questa tecnologia molto promettente per lo sviluppo di una nuova classe di analgesici con un profilo di sicurezza favorevole. Una volta digerito il risultato, la comunità scientifica ha iniziato a mettere in discussione la logica alla base del risultato di Pfizer. Uno dei pionieri della farmacologia dell'anandamide, Vincenzo Di Marzo, ha esplorato in un tipico editoriale le stile diverse ragioni per cui il controllo del dolore attraverso la stimolazione del tono endocannabinoide potrebbe non essere così facile come inizialmente previsto.2 Una delle argomentazioni principali avanzate da Di Marzo nel suo commento è che i cannabinoidi hanno dimostrato efficacia nelle condizioni di dolore cronico in cui i pazienti hanno un grado di ansia più elevato. Anche gli sperimentatori di Pfizer hanno suggerito che la scarsa componente affettiva del modello utilizzato può aver contribuito alla mancanza di efficacia dimostrata dal PF-04457845. Questo mi ha ricordato un lavoro che avevo letto un paio di anni prima, quando ero uno studente di dottorato, in cui esperti nell'elaborazione neurologica del dolore spiegavano che i ratti e altri mammiferi inferiori semplicemente non possiedono le strutture neuroanatomiche responsabili dell'elaborazione del dolore negli esseri umani.3 All'epoca non ci feci molto caso perché ero in dirittura d'arrivo del mio dottorato e l'ultima cosa a cui si vuole pensare prima di difendere la tesi è quanto sia realmente utile ciò che si sta facendo. Ma da quando ho iniziato a lavorare con i pazienti che utilizzano la cannabis terapeutica, questo effetto modulatore del sistema endocannabinoide sulla componente affettiva del dolore cronico è diventato una delle chiavi per spiegare gli effetti osservati nella pratica clinica.
Intensità del dolore, soglia del dolore e sofferenza.
Le evidenze attuali indicano chiaramente che l'esperienza del dolore cronico negli esseri umani è composta da dimensioni sia sensoriali che affettive ed è spesso accompagnata dal desiderio di porre fine al dolore, di ridurlo, o di sfuggirgli. Questa dimensione affettiva del dolore è in parte costituita da emozioni riferite al presente o al futuro prossimo del paziente, come l'angoscia o la paura. Un'altra componente affettiva del dolore, l'"affetto secondario", è costituita da sentimenti motivati dalle implicazioni a lungo termine del dolore cronico, come la sofferenza. L'affetto secondario si basa su una riflessione più elaborata, influenzata dal ricordo, dalla memoria e dall'anticipazione, sulla perdita di autonomia e di qualità della vita, sulle difficoltà di sopportare il dolore a lungo termine e sulle implicazioni per il futuro e la sopravvivenza del paziente. Pertanto, il dolore cronico è spesso vissuto non solo come una minaccia allo stato attuale del corpo, al benessere o all'attività quotidiana, ma anche al benessere futuro e alla vita in generale.4
Ma qual è l'effetto dei cannabinoidi sulla componente affettiva del dolore? Una meta-analisi di studi di laboratorio sull'uomo, in cui i trattamenti vengono testati su volontari sani sottoposti a stimoli dolorosi piuttosto che su pazienti reali, ha concluso che la somministrazione di farmaci a base di cannabinoidi previene l'insorgenza del dolore producendo leggeri aumenti della soglia del dolore, ma non riduce l'intensità del dolore già provato. I cannabinoidi rendevano invece il dolore meno spiacevole e più tollerabile per i partecipanti, suggerendo un effetto sull'elaborazione emotiva del dolore.5 In uno degli esperimenti inclusi in questa meta-analisi, i partecipanti che hanno ricevuto THC in combinazione con morfina hanno descritto un effetto sinergico sulla riduzione del disagio percepito, ma non sull'intensità del dolore. Gli autori hanno interpretato queste due componenti utilizzando la similitudine di una radiolina: una dimensione corrisponde al volume, più o meno alto, al quale si ascolta la radio. L'altro corrisponde quanto questa radiolina dia fastidio, che è un valore soggettivo, più qualitativo che quantitativo, e che può essere o meno correlato al volume o all'intensità.6 Questo risultato è coerente con quelli ottenuti in studi osservazionali su pazienti cronici che ricevono un trattamento con cannabis terapeutica, che riportano un lieve effetto sull'intensità del dolore percepito, ma un robusto impatto sulla qualità di vita correlata alla salute e un importante miglioramento delle comorbidità psichiatriche come la qualità dell'umore, dell'ansia, dello stress o del sonno.7
La memoria del dolore
Ma come fanno i cannabinoidi a modulare selettivamente la componente affettiva del dolore? Anche se la risposta non è ancora chiara, abbiamo alcune indicazioni ricavate da studi di neuroimaging in cui i partecipanti sono sottoposti a uno stimolo doloroso. In questi si osserva che la somministrazione di THC può bloccare l'aumento dell'attività neuronale nella corteccia cingolata anteriore (ACC), una struttura cerebrale responsabile del trasferimento delle informazioni sul dolore ai nuclei superiori, dove vengono integrate con i ricordi e le esperienze per elaborare le risposte affettive. È proprio questa via che manca negli animali inferiori come i ratti, che producono una risposta molto più immediata e meno elaborata agli stimoli dolorosi.8 Allo stesso modo, sappiamo che l'attivazione del recettore 1 dei cannabinoidi, il bersaglio comune dell'anandamide e del THC, in un'altra area del cervello chiamata amigdala, svolge un ruolo chiave nell'estinguere i ricordi avversivi associati a esperienze negative o traumatiche. Le esperienze ripetute rimangono impresse nella memoria e le continue esperienze dolorose generano un ricordo del dolore. La paura e il dolore giocano un ruolo dominante nella vita dei pazienti cronici che vivono continuamente nell'aspettativa che il dolore si manifesti. Gli esperti sottolineano l'importanza di affrontare questa paura generando spazi privi di dolore e sviluppando così nel paziente una sensazione di controllo, che contribuisce anche a ridurre il suo stato generale di ansia. Forse questo potrebbe essere uno dei motivi per cui i cannabinoidi, attraverso il controllo dell'elaborazione delle componenti affettive degli stimoli dolorosi e l'estinzione dei ricordi negativi associati al dolore cronico, potrebbero essere più efficaci in quei pazienti con comorbidità psichiatriche come stress, ansia e depressione, che costituiscono la maggior parte dei pazienti che soffrono di dolore cronico. Le evidenze disponibili sembrano indicare che l'uso continuato di cannabinoidi in questo tipo di pazienti è in grado di migliorare comportamenti come la catastrofizzazione e la rimuginazione sia diurna che notturna, facilitando così l'accettazione, la resilienza e i pensieri positivi sulla propria salute (vedi figura).9
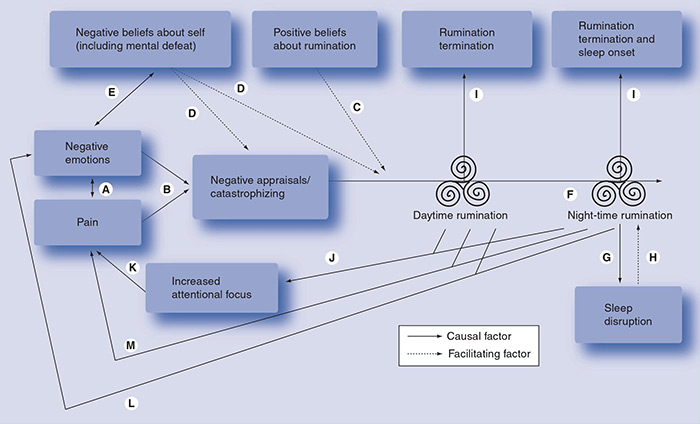
| Negative beliefs about self (including mental defeat) | Opinioni negative su di sé (compreso disfattismo mentale) |
| Positive beliefs about rumination | Opinioni positive sulla rimuginazione |
| Rumination termination | Fine della rimuginazione |
| Rumination termination and sleep onset | Fine della rimuginazione ed inizio del sonno |
| Negative emotions | Emozioni negative |
| Pain | Dolore |
| Negative appraisals / catastrophizing | Valutazioni negative / catastrofizzazione |
| Daytime rumination | Rimuginazione diurna |
| Night-time rumination | Rimuginazione notturna |
| Increased attentional focus | Aumento della focalizzazione dell'attenzione |
| Sleep disruption | Disturbi del sonno |
| Causal factor | Fattore causante |
| Facilitating factor | Fattore facilitante |
Queste aree cerebrali, l'ACC e l'amigdala, sono anche implicate nell'elaborazione anomala degli stimoli avversivi nei pazienti psichiatrici. Studi osservazionali hanno identificato un aumento significativo della comunicazione tra queste due regioni durante i processi emotivi legati alla paura nei pazienti con diagnosi di disturbi d'ansia, ma non nei volontari sani. Inoltre, questo aumento dell'attività cerebrale è risultato positivamente correlato ai sintomi ansiosi descritti dai pazienti.10 Per questo motivo, i farmaci a base di cannabis possono rappresentare un'aggiunta efficace a un piano di gestione farmacologica multimodale non solo per il dolore cronico, ma anche per altre condizioni croniche debilitanti con una componente traumatica, come i disturbi d'ansia, l'ansia sociale o generalizzata, o il disturbo da stress post-traumatico.
Un sospiro di sollievo
Ma in cosa si traduce per il paziente tutta questa modulazione dei processi neuronali? In studi qualitativi in cui viene registrata l'esperienza dei pazienti che fanno uso di cannabis a scopo terapeutico, ci sono due figure ricorrenti, comuni alla maggior parte dei resoconti: la prima è il "sospiro di sollievo", un'espressione che i pazienti usano comunemente per descrivere l'effetto che provano dopo aver inalato la cannabis. Una sensazione di rilassamento corporeo e mentale che permette al paziente di accedere a una seconda sensazione, quella del "ripristino del sé"11 I pazienti descrivono come l'uso della cannabis terapeutica permetta loro di riconnettersi con se stessi, con la persona che erano prima di ammalarsi, di svolgere attività quotidiane che davano loro piacere, come prendersi cura delle piante, fare una passeggiata con la famiglia o uscire a cena. In breve, di migliorare la qualità di vita legata alla salute, quel delicato equilibrio tra paura della malattia e amore della propria esistenza.
1. Huggins, J. P., Smart, T. S., Langman, S., Taylor, L. & Young, T. An efficient randomised, placebo-controlled clinical trial with the irreversible fatty acid amide hydrolase-1 inhibitor PF-04457845, which modulates endocannabinoids but fails to induce effective analgesia in patients with pain due to osteoarthritis of the knee. Pain 153, 1837-1846 (2012).
2. Di Marzo, V. Inhibitors of endocannabinoid breakdown for pain: not so FA(AH)cile, after all. Pain 153, 1785-1786 (2012).
3. Craig, A. D. A rat is not a monkey is not a human: Comment on Mogil (Nature Rev. Neurosci. 10, 283-294 (2009)). Nat. Rev. Neurosci. 10, 466 (2009).
4. Price, D. D. Psychological and Neural Mechanisms of the Affective Dimension of Pain. Science (80-. ). 288, 1769-1772 (2000).
5. De Vita, M. J., Moskal, D., Maisto, S. A. & Ansell, E. B. Association of Cannabinoid Administration With Experimental Pain in Healthy Adults: A Systematic Review and Meta-analysis. JAMA psychiatry 75, 1118-1127 (2018).
6. Roberts, J. D., Gennings, C. & Shih, M. Synergistic affective analgesic interaction between delta-9- tetrahydrocannabinol and morphine. Eur. J. Pharmacol. 530, 54-58 (2006).
7. Moreno-Sanz, G., Madiedo, A., Lynskey, M. & Brown, M. R. D. 'Flower Power': Controlled Inhalation of THC-Predominant Cannabis Flos Improves Health-Related Quality of Life and Symptoms of Chronic Pain and Anxiety in Eligible UK Patients. Biomed. 2022, Vol. 10, Page 2576 10, 2576 (2022).
8. Lee, M. C. et al. Amygdala activity contributes to the dissociative effect of cannabis on pain perception. Pain 154, 124-134 (2013).
9. Edwards, M. J., Tang, N. K., Wright, A. M., Salkovskis, P. M. & Timberlake, C. M. Thinking about thinking about pain: a qualitative investigation of rumination in chronic pain. http://dx.doi.org/10.2217/pmt.11.29 1, 311-323 (2011).
10. Robinson, O. J. et al. The dorsal medial medial prefrontal (anterior cingulate) cortexâ€"amygdala aversive amplification circuit in unmedicated generalised and social anxiety disorders: an observational study. The Lancet Psychiatry 1, 294-302 (2014).
11. Lavie-Ajayi, M. & Shvartzman, P. Restored Self: A Phenomenological Study of Pain Relief by Cannabis. Pain Med. 20, 2086-2093 (2019).


