Par Tanja Bagar

Le Dr Tanja Bagar est une microbiologiste titulaire d'un doctorat en biomédecine. Elle a acquis une vaste expérience de la recherche en biotechnologie, en biologie moléculaire et en signalisation cellulaire dans des laboratoires en Slovénie, en Allemagne et au Royaume-Uni. Elle s'est principalement concentrée sur le système endocannabinoïde et les substances actives du cannabis/chanvre. Ses travaux ont conduit à la création de l'Institut international des cannabinoïdes (ICANNA), dont elle est directrice générale et présidente du conseil d'experts. Elle est également directrice adjointe et responsable de la R&D dans une société environnementale. Elle est également active dans la sphère universitaire. Elle donne des conférences dans le domaine de la microbiologie et est la doyenne du programme de maîtrise en écomédiation de la faculté Alma Mater Europaea.

Le cannabidiol (CBD) est l'un des cannabinoïdes les plus présents dans la plante Cannabis sativa L. En 2018, un rapport d'examen critique a été publié par l'Organisation mondiale de la santé, qui a constaté, à travers un certain nombre d'essais contrôlés et ouverts, que le CBD est généralement bien toléré, présente un bon profil d'innocuité et ne présente pas de risque d'abus.
Le CBD présente un vaste spectre d'effets biologiques, offrant des bienfaits potentiels pour plusieurs pathologies telles que l'anxiété, l'inflammation, les douleurs neuropathiques et les affections neurologiques. Les recherches actuelles suggèrent que le CBD agit sur de différentes cibles dans l'organisme et que ses effets sont par conséquent attribuables à plusieurs mécanismes d'action moléculaires. Le CBD stimule plusieurs récepteurs et en module de nombreux autres; il se lie également à des enzymes et influe sur leur activité. Par exemple, le CBD a un effet ralentisseur sur le groupe d'enzymes cytochrome P450 dans le foie, et c'est la raison pour laquelle nous devons être prudents lorsque nous combinons le CBD avec certains médicaments, car le cytochrome P450 est responsable de l'élimination de nombreux médicaments dans notre organisme. Cette large interaction avec les récepteurs, les enzymes, les canaux ioniques et les transporteurs permet d'affirmer que le CBD exerce une influence sur plus d'une centaine de cibles moléculaires dans l'organisme. Pour le moment, l'efficacité clinique du CBD est encore incertaine. Les données issues d'essais cliniques randomisés, de modèles in vitro et in vivo et d'observations cliniques en situation réelle soutiennent l'utilisation du CBD pour de nombreuses pathologies et situations cliniques. Dans la pratique clinique, nous observons souvent chez les patients des bienfaits qui vont au-delà de meilleurs résultats cliniques : cela est dû à ce vaste réseau d'interactions.
L'être humain possède une architecture génétique extraordinaire, on estime que 20 000 à 25 000 gènes sont codés dans notre ADN. Toutes les données se rapportant à chacun d'entre nous y sont stockées. Chaque cellule contient des données sur l'ensemble de l'organisme. Fait remarquable, malgré la grande complexité de la physiologie humaine, le nombre de gènes que nous possédons est comparable, et parfois inférieur, à celui des autres espèces. Par exemple, le nématode (Caenorhabditis elegans) possède à peu près autant de gènes que l'être humain (environ 20 000) et certaines plantes, comme le riz (Oryza sativa), ont presque deux fois plus de gènes que l'être humain, soit environ 40 000. La Paris japonica, une plante à fleurs originaire du Japon, détient le record du plus grand génome répertorié, qui est environ 50 fois supérieur au génome humain.
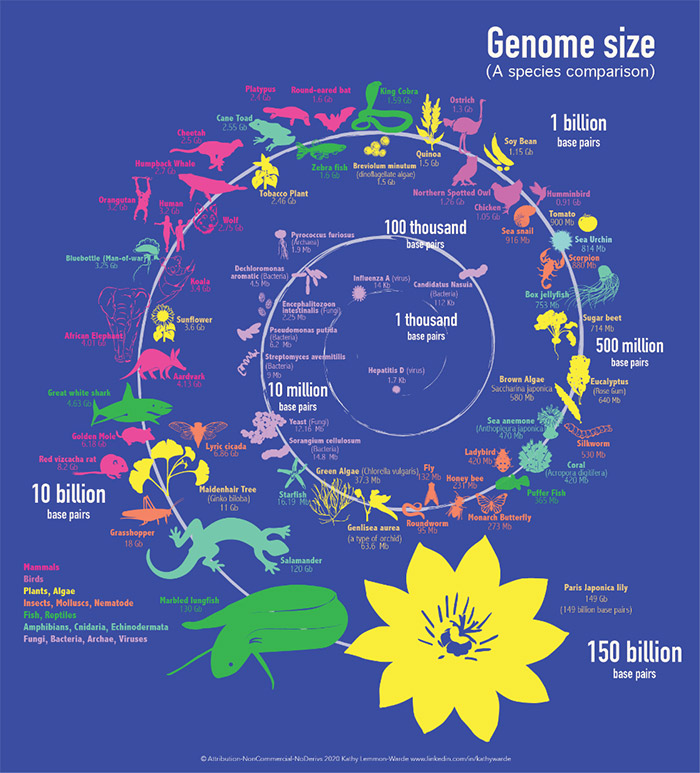
Régulation génique
Bien que l'être humain ne compte pas le plus grand génome, il est considéré comme l'un des organismes les plus complexes en termes de biochimie, d'anatomie, de cognition et de comportement. Notre complexité ne provient pas de la quantité de gènes, mais de la manière dont ces gènes sont régulés, exprimés et interagissent au sein de divers réseaux biologiques. Nous disposons de mécanismes de régulation génique très complexes, qui déterminent si les gènes sont activés ou inhibés, garantissant ainsi que les fonctions biologiques interviennent au bon moment, au bon endroit et avec l'intensité appropriée. Bien que le nombre de gènes soit similaire pour tous les mammifères, les différences dans la régulation génique sont déterminantes pour l'unicité de chaque espèce. Dans chaque cellule, seul un ensemble spécifique de gènes est actif, et l'expression génique doit être étroitement régulée en réponse à des signaux internes et externes. Les mécanismes principaux impliqués dans la régulation génique comprennent les modifications épigénétiques (ces modifications agissent comme des interrupteurs ou des gradateurs qui régissent l'activité ou l'inactivité d'un gène, sans modifier le gène lui-même), les facteurs de transcription (protéines qui se fixent sur des parties spécifiques de l'ADN pour stimuler ou inhiber ce gène) et les microARN (petites molécules qui contrôlent l'activité d'un gène).
Une régulation génique adéquate est cruciale pour la préservation de la santé cellulaire et de la santé globale. Un dérèglement de l'expression génique peut entraîner divers symptômes ainsi qu'une prolifération cellulaire incontrôlée (par exemple dans le cas d'un cancer) ou la mort des cellules, ce qui contribue à l'apparition de diverses maladies.
Le CBD et l'expression génique
Chez l'être humain, la régulation génique est influencée par divers facteurs, dont l'environnement, le régime alimentaire et certaines substances végétales comme le cannabidiol (CBD). Il a été démontré que le CBD affecte l'expression génique en interagissant avec certaines voies moléculaires. Un mécanisme particulier permettant au CBD d'exercer ses effets est son interaction avec un récepteur spécifique, le récepteur gamma activé par les proliférateurs de peroxysomes (PPARγ). Le PPARγ en tant que facteur de transcription est impliqué dans la régulation du métabolisme du glucose, du stockage des acides gras et de la sensibilité à l'insuline. Il module également les réponses à l'inflammation et au stress oxydatif. Lorsque le PPARγ est activé, il se lie à des séquences d'ADN spécifiques connues sous le nom d'éléments de réponse PPAR (PPRE), qui régulent la transcription des gènes impliqués dans ces processus biologiques vitaux. Le rôle du PPARγ est particulièrement important dans le cas de certaines des maladies les plus répandues dans la société moderne, comme le diabète de type 2, l'obésité, le cancer et les maladies neurodégénératives.
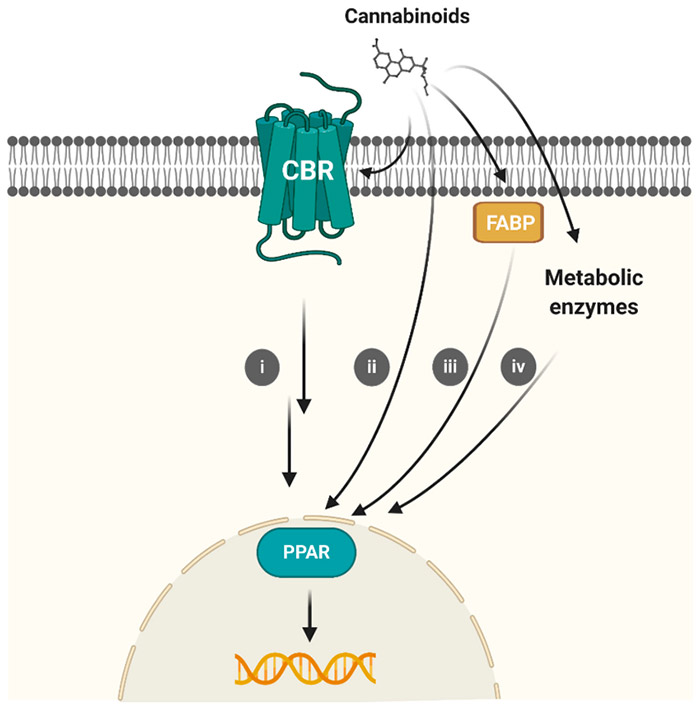
Cette capacité du CBD à activer le PPARγ a d'abord été mise en évidence dans plusieurs études qui ont démontré les propriétés anti-inflammatoires et neuroprotectrices du CBD. Il a été démontré que le CBD se lie au PPARγ et l'active, entraînant une régulation à la hausse des gènes qui stimulent les effets anti-inflammatoires et protègent contre les lésions neuronales. Cette interaction est déterminante dans des maladies telles que l'épilepsie, la maladie d'Alzheimer et la maladie de Parkinson, où la neuroinflammation et le stress oxydatif contribuent à la progression de la maladie.
De plus, l'activation du PPARγ par le CBD a été associée à une inhibition de la prolifération des cellules cancéreuses et des métastases. Des études ont démontré que l'activation du PPARγ peut induire l'arrêt du cycle cellulaire et l'apoptose (mort cellulaire programmée) dans certains types de cellules cancéreuses, ce qui suggère que les propriétés anticancéreuses du CBD pourraient agir, du moins en partie, par l'intermédiaire de cette voie.
Étant donné que les récepteurs cannabinoïdes et les PPAR, en particulier le CB2R et le PPARγ, présentent un intérêt biologique dans des états physiopathologiques communs, les chercheurs ont également exploré des stratégies de ciblage multiple, dans lesquelles les récepteurs cannabinoïdes et les PPARγ sont ciblés simultanément, ce que l'on appelle le « double ciblage ». Dans le cas du CB2R et du PPARγ, cette approche est apparue comme une stratégie thérapeutique prometteuse en raison des rôles complémentaires que jouent ces récepteurs dans la régulation de l'inflammation, des réponses immunitaires et des processus métaboliques. Ce double ciblage du CB2R et du PPARγ vise à améliorer l'efficacité thérapeutique en modulant à la fois les voies immunitaires et métaboliques. Cette stratégie a été étudiée dans diverses conditions, notamment dans les maladies neurodégénératives (comme les maladies d'Alzheimer et de Parkinson), les maladies auto-immunes (comme la sclérose en plaques) et les troubles métaboliques (comme l'obésité et le diabète). Des études précliniques ont révélé que l'activation combinée du CB2R et du PPARγ pouvait avoir des avantages synergiques, de sorte qu'une approche multicible combinée peut constituer une stratégie précieuse dans le traitement de certaines maladies chroniques. Voici une liste des domaines dans lesquels des recherches très prometteuses ont déjà été réalisées.
- Syndrome métabolique et diabète de type 2
Le syndrome métabolique et le diabète de type 2 sont de plus en plus répandus dans la société moderne; de nombreux nouveaux cas apparaissent chaque année et les populations les plus jeunes sont touchées. L'utilisation du CBD pour moduler le récepteur cannabinoïde de type 2 et cibler le PPARγ permet notamment de lutter contre l'inflammation et d'agir sur le métabolisme du glucose. Cela peut contribuer à réguler le métabolisme lipidique, à améliorer la sensibilité à l'insuline et à réduire l'inflammation chronique, offrant ainsi potentiellement des résultats thérapeutiques mieux équilibrés que si l'on cible uniquement l'un ou l'autre des récepteurs. - Anxiété et TSPT
Des effets significatifs du cannabidiol ont été observés au niveau de la consolidation de la mémoire liée à la peur, en particulier en ce qui concerne la réduction de l'expression de la mémoire liée à la peur et l'amélioration du processus d'extinction de la peur. Des recherches suggèrent que le CBD pourrait contribuer à perturber la reconsolidation des souvenirs liés à la peur ou à renforcer le processus d'extinction, deux éléments essentiels dans la gestion de maladies telles que le syndrome de stress post-traumatique (TSPT) et d'autres troubles anxieux. Les récepteurs cannabinoïdes (CB1 et CB2) et les PPARγ jouent un rôle majeur dans la réponse du cerveau à la peur et à l'anxiété, et sont donc des cibles importantes à prendre en compte dans le traitement de l'anxiété et du syndrome de stress post-traumatique (TSPT). - Perméabilité de la barrière hématoencéphalique (BHE) à la suite d'une ischémie (comme un accident vasculaire cérébral)
L'ischémie entraîne souvent une dégradation de la BHE, ce qui augmente sa perméabilité et permet aux substances nocives et aux cellules immunitaires de pénétrer dans le cerveau, ce qui exacerbe l'inflammation et les lésions neuronales dans le cerveau. Des études indiquent que le CBD peut stabiliser la BHE et réduire sa perméabilité en agissant sur les récepteurs cannabinoïdes et PPARγ. Cet effet protecteur est en partie dû à sa capacité à réduire la neuroinflammation et à ses propriétés antioxydantes, lesquelles renforcent ses effets protecteurs. Les recherches démontrent que le CBD constitue un agent thérapeutique potentiel pour les pathologies dans lesquelles le maintien de la fonction de la BHE est crucial pour la guérison. - Sclérose/sclérodermie systémique
Dans le cas de maladies auto-immunes telles que la sclérodermie systémique (ScS), caractérisée par une inflammation excessive, une fibrose et un dérèglement du système immunitaire, il serait possible de réduire la fibrose et l'hyperactivité immunitaire en ciblant à la fois le CB2R et le PPARγ. L'activation du CB2R réduit l'infiltration des cellules immunitaires et l'inflammation, tandis que le PPARγ contribue à la régulation de la fibrose en inhibant la production de collagène, une des caractéristiques de la sclérodermie. - Sclérose en plaques (SP)
Chez les personnes atteintes de sclérose en plaques, une maladie auto-immune caractérisée par l'atteinte du système nerveux central par le système immunitaire, le CB2R et le PPARγ présentent des bienfaits complémentaires. L'activation du CB2R limite les lésions d'origine immunologique, réduisant la neuroinflammation, tandis que le PPARγ module l'activité des microglies et la neuroinflammation, contribuant ainsi à la protection neuronale. Des études ont démontré que les agonistes PPARγ réduisent la démyélinisation et renforcent la neuroprotection, rendant cette approche de double ciblage particulièrement prometteuse pour la SP. - Maladie d'Alzheimer (MA)
Chez les personnes atteintes de la maladie d'Alzheimer, la neuroinflammation et le stress oxydatif jouent un rôle crucial dans la progression de la maladie. L'activation des récepteurs cannabinoïdes et des PPARγ a démontré des effets neuroprotecteurs. Le CBD réduit l'activation des microglies et l'inflammation, tandis que l'activation du PPARγ contribue à la gestion du stress oxydatif, à la stimulation de la clairance de la bêta-amyloïde et à l'amélioration de la fonction mitochondriale, qui sont tous des éléments essentiels pour freiner l'évolution de la maladie d'Alzheimer. - Cancer
Dans le cas du cancer, le double ciblage du CB2R et du PPARγ peut inhiber la progression de la tumeur par le biais de mécanismes anti-inflammatoires, antiprolifératifs et proapoptotiques. Il a été démontré que l'activation du récepteur cannabinoïde de type 2 dans les cellules cancéreuses réduit la croissance tumorale en inhibant la prolifération et en favorisant l'apoptose. Le PPARγ possède des propriétés antitumorales similaires, notamment l'inhibition de la croissance cellulaire, la réduction des métastases et l'induction de la mort dans les cellules cancéreuses. Combinées, ces voies pourraient représenter une approche synergique à prendre en considération dans le traitement du cancer, en particulier dans les cancers associés à une inflammation chronique.
Conclusions
La capacité du CBD à influer sur la régulation génique, notamment par le biais de son interaction avec le PPARγ, laisse entrevoir des possibilités intéressantes d'interventions thérapeutiques. L'activation du PPARγ par le CBD s'avère prometteuse dans le traitement d'un large éventail de pathologies. De nouvelles recherches nous permettent de mieux comprendre les mécanismes moléculaires qui sous-tendent la capacité du CBD à moduler l'expression génique. À mesure que la recherche progresse, le rôle du CBD dans la régulation génique pourrait déboucher sur de nouvelles thérapies ciblées pour soigner des maladies complexes, offrant ainsi de l'espoir aux patients souffrant de pathologies qui s'avéraient jusqu'à présent difficiles à traiter. Toutefois, bien que les études précliniques soient prometteuses, des recherches cliniques supplémentaires sont nécessaires pour mieux comprendre le potentiel du CBD et les effets de ces modifications du profil d'expression génique. Il est indispensable de déterminer comment la modulation des gènes par le CBD influe sur les résultats de santé à long terme, en particulier dans le cas de maladies multifactorielles complexes telles que le cancer, la neurodégénérescence et les maladies auto-immunes. De plus, la variation des réactions individuelles au CBD, influencées par des facteurs tels que la génétique, le dosage et les méthodes d'administration, doit être soigneusement étudiée afin d'optimiser son utilisation thérapeutique. Les progrès de la science permettront de mieux comprendre comment le CBD peut être intégré dans des approches personnalisées visant à optimiser la santé. Le CBD est susceptible de redéfinir et d'améliorer la gamme des traitements médicaux, mais il convient de disposer de preuves rigoureuses pour pouvoir transposer les nouvelles connaissances en matière de molécules dans des traitements axés sur les patients.
Références
Khosropoor S, Alavi MS, Etemad L, Roohbakhsh A. Cannabidiol Goes Nuclear: The Role of PPARγ. Phytomedicine. 2023; DOI: 10.1016/j.phymed.2023.154771.
O'Sullivan SE. An update on PPAR activation by cannabinoids. Br J Pharmacol. 2016 Oct;173(12):1899-910. doi: 10.1111/bph.13497. PMID: 26585190; PMCID: PMC4911841.
Lago-Fernandez A, Zarzo-Arias S, Jagerovic N, Morales P. Relevance of Peroxisome Proliferator Activated Receptors in Multitarget Paradigm Associated with the Endocannabinoid System. International Journal of Molecular Sciences. 2021; 22(3):1001. https://doi.org/10.3390/ijms22031001
Esposito G, Scuderi C, Valenza M, Togna GI, Latina V, De Filippis D, Cipriano M, Carratù MR, Iuvone T, Steardo L. Cannabidiol reduces Aβ-induced neuroinflammation and promotes hippocampal neurogenesis through PPARγ involvement. PLoS One. 2011;6(12). doi: 10.1371/journal.pone.0028668. PMID: 22163051; PMCID: PMC3226620.
Granja AG, Carrillo-Salinas FJ, Pagani A, Gómez-Cañas M, Negri R, Navarrete C, Mecha M, Mestre L, Fiebich BL, Cantarero I, Tolón RM, Hillard CJ, Guaza C. A Cannabidiol (CBD) derivative attenuates experimental autoimmune encephalomyelitis by modulating the PPARγ pathway. Neuropharmacology. 2019 Jan;144:159-169. doi: 10.1016/j.neuropharm.2018.10.026. PMID: 30389361.
Fernández-Ruiz J, Moro MA, Martínez-Orgado J. Cannabinoids in neurodegenerative disorders and stroke/brain trauma: from preclinical models to clinical applications. Neurotherapeutics. 2015 Oct;12(4):793-806. doi: 10.1007/s13311-015-0373-0. PMID: 26347359; PMCID: PMC4633651.
Ramer R, Heinemann K, Merkord J, Rohde H, Salamon A, Linnebacher M, Hinz B. COX-2 and PPAR-γ confer cannabidiol-induced apoptosis of human lung cancer cells. Mol Cancer Ther. 2013 Jan;12(1):69-82. doi: 10.1158/1535-7163.MCT-12-0335. PMID: 23108619.
Patsenker E, Stoll M, Millonig G, Agaimy A, Wissniowski TT, Schneider V, Mueller S, Bartsch B, Brenneisen R, Zimmer A, Stickel F. Cannabinoid receptor type I modulates alcohol-induced liver fibrosis. Hepatology. 2011 Jul;54(1):196-206. doi: 10.1002/hep.24332. PMID: 21538442.


