Por Andrew F Scheyer

Andrew F Scheyer es becario posdoctoral en el Institut de Neurobiologie de la Méditerranée en Marsella, Francia, en el laboratorio del Dr. Olivier J Manzoni. Se especializa en electrofisiología y es un apasionado de la comunicación científica. Antes de trabajar en su puesto actual, Andrew completó su doctorado sobre el tema de los mecanismos sinápticos subyacentes a la adicción a la cocaína y la abstinencia en 2015 en el laboratorio de Marina E Wolf en la Universidad Rosalind Franklin en North Chicago, en Estados Unidos. Desde entonces, su investigación se ha centrado en la trayectoria de desarrollo del sistema endocannabinoide y cómo se ve afectado por la exposición prenatal y posnatal temprana al cannabis. Sus publicaciones recientes en Trends in Neurosciences and Biological Psychiatry se centran en las alteraciones del desarrollo neurológico y los comportamientos de la vida temprana después de la exposición perinatal al cannabis. Cuando no está en el laboratorio, Andrew practica el ciclismo de distancia ultralarga y es un jardinero entusiasta.
A medida que la reevaluación global actual del consumo de cannabis continúa su tendencia hacia la despenalización y la legalización, a la vez se debe de efectuar una sincera evaluación de los riesgos del consumo de cannabis. Si bien muchas discusiones ya han resaltado los peligros del consumo de cannabis durante los períodos críticos del desarrollo del cerebro, como la infancia y la adolescencia, se ha prestado poca atención al consumo de cannabis durante el embarazo y el período posnatal temprano (es decir, durante la lactancia). Sin embargo, sabemos que los principios activos del cannabis, como el THC y el CBD, se transfieren al feto en desarrollo cuando las mujeres los usan durante el embarazo. Al igual que con otras drogas, esta exposición tiene el potencial de afectar significativamente al bebé en desarrollo, dejando marcas duraderas que alterarán su vida incluso antes de que haya entrado en el mundo.
Actualmente, el 70 % de las mujeres encuestadas en Estados Unidos creen que existe un "riesgo leve o nulo" asociado con el consumo de cannabis durante el embarazo1. La percepción del cannabis como alternativa natural a las drogas farmacéuticas lo posiciona como un remedio más fácil y aparentemente más benigno para muchas de las enfermedades asociadas con el embarazo, tales como náuseas, ansiedad, malestar físico e inquietud. Además, en un estudio reciente en el estado estadounidense de Colorado, donde el cannabis está legalizado para uso de forma tanto recreativa como médica, se observó que casi el 70% de los dispensarios de cannabis recomiendan el uso de cannabis durante el primer trimestre del embarazo para combatir las náuseas entre estos otras molestias asociadas con el embarazo2. Sin embargo, tanto la investigación de laboratorio como los estudios en seres humanos que han usado cannabis durante el embarazo han demostrado que existen consecuencias negativas significativas derivadas de este uso.
El consumo de cannabis durante el embarazo conlleva riesgos significativos debido a la participación del sistema endocannabinoide en muchos procesos cruciales del desarrollo. Brevemente, el sistema endocannabinoide es un sistema biológico que se encuentra en todo el cuerpo y el cerebro formado por neurotransmisores y receptores que sirve para ajustar casi todas las funciones fisiológicas y cognitivas, desde la frecuencia cardíaca y la digestión hasta tareas mentales complejas como la memoria y el comportamiento social. Los principios activos del cannabis funcionan al interaccionar con este mismo sistema, lo que explica por qué los efectos del cannabis se extienden tanto por el cuerpo y el cerebro. El sistema endocannabinoide es un participante crucial en muchos pasos importantes del desarrollo, desde la fertilización de los óvulos hasta la organización más temprana de las regiones cerebrales nacientes. Cuando el cannabis es utilizado por una madre embarazada o en período de lactancia, y sus principios activos se transmiten al feto o al bebé en desarrollo, estos procesos se interrumpen, lo que da como resultado una serie de consecuencias.
La investigación sobre las consecuencias del consumo de cannabis durante el embarazo se realiza a través de dos vías principales: estudios epidemiológicos (aquellos que recopilan datos de poblaciones humanas) e investigación de laboratorio utilizando modelos animales. Es importante destacar que existe una notable coherencia entre los estudios realizados en roedores y los efectos observados en humanos, que en el presente documento se destacan en la Figura 1. Si bien dicho acuerdo entre el modelado controlado en laboratorio de los trastornos y las afecciones del mundo real no es universal entre las actividades científicas, los datos que se han producido en modelos de consumo de cannabis en roedores durante el embarazo no solo han confirmado lo que se ve en humanos expuestos al cannabis en el útero, sino que también han proporcionado perspectivas valiosas e importantes sobre los mecanismos moleculares y celulares subyacentes a estos efectos, que son difíciles de determinar con técnicas o invasivas en seres humanos. Por otro lado, los parámetros cognitivos complejos, como el comportamiento social y la planificación de tareas, que son difíciles de observar en los animales, se han investigado de manera sólida en los estudios epidemiológicos. Por lo tanto, los dos brazos de investigación trabajan para complementarse entre sí y proporcionar una imagen más completa de las consecuencias de la exposición prenatal al cannabis.
Estudios en seres humanos
En el frente epidemiológico, hasta ahora tres estudios principales han documentado los resultados del consumo de cannabis durante el embarazo en el desarrollo de los hijos de estas usuarias. En primer lugar, el Estudio Prospectivo Prenatal de Ottawa (OPPS, por sus siglas en inglés), que se inició en 1978, examinó a mujeres embarazadas de clase media europeas de bajo riesgo y realizó un seguimiento de sus hijos hasta la edad adulta temprana (18-22 años)3-6 . Por otra parte, el estudio de Prácticas de salud materna y desarrollo infantil (MHCPD, por sus siglas en inglés) se centró en mujeres embarazadas de alto riesgo de etnia mixta y nivel socioeconómico bajo, y realizó el seguimiento de sus hijos hasta la adolescencia (14 años de edad)7-11. Finalmente, en el estudio Generación R, que está en curso, participaron mujeres embarazadas de un nivel socioeconómico medio a alto y continúa realizando el seguimiento de la descendencia12-13.
Por consiguiente ¿qué han descubierto estos estudios epidemiológicos? A diferencia de la exposición prenatal al alcohol o al cigarrillo, los efectos del consumo de cannabis durante el embarazo se manifiestan principalmente como problemas conductuales y cognitivos. En todos estos estudios se han observado pesos bajos al nacer, aunque no se observan otras anomalías graves en la descendencia de las madres que consumen cannabis. La inteligencia, medida por pruebas estandarizadas como el coeficiente intelectual y los puntos de referencia de la vida temprana, rara vez se ve afectada por la exposición al cannabis en el útero. Si bien el MHPCD informó sobre un desarrollo mental lento durante el primer año, estos efectos casi no existían durante la mitad de su segundo año. Tanto el MHPCD como el OPPS descubrieron que la función verbal y de memoria en los niños pequeños es deficiente cuando han estado expuestos al cannabis durante el embarazo.
Los hallazgos más consistentes están relacionados con la impulsividad y la hiperactividad. A los 6 y 10 años de edad, tanto el OPPS como el MHPCD informaron sobre un aumento en estos comportamientos, que también se observó de manera en el estudio de la Generación R, que informó que a esta edad los niños tenían más probabilidades de exhibir un comportamiento agresivo y de infracción de las reglas que sus compañeros. Estos cambios de comportamiento tampoco se detienen durante la infancia: los hijos de madres que consumieron cannabis durante el embarazo tienen más probabilidades de abusar de drogas como los opiáceos, el tabaco y el cannabis que sus pares, y comienzan este uso más temprano en la vida. La función cerebral anormal asociada con una memoria de trabajo deficiente también se encuentra cuando estos descendientes alcanzan la edad adulta. Por lo tanto, los datos adquiridos de los estudios epidemiológicos de seres humanos expuestos al cannabis durante el embarazo han revelado déficit significativos y duraderos que comienzan en el nacimiento y persisten hasta la edad adulta.
Modelos animales
La investigación de laboratorio, utilizando modelos animales de consumo de cannabis durante el embarazo y la lactancia, ha respaldado y ampliado estos hallazgos. Sin embargo, a diferencia de la investigación en seres humanos, los modelos animales pueden proporcionar información sobre cómo los déficit de comportamiento causados por la exposición al cannabis se correlacionan con cambios específicos en la estructura y función del cerebro. Al igual que con los seres humanos, el comportamiento social y emocional en la vida temprana se ve perturbado por la exposición al cannabis durante el embarazo14-15. Estas interrupciones son causadas por cambios en una región del cerebro conocida como corteza prefrontal, que es responsable de muchas de las llamadas "funciones ejecutivas", como el pensamiento crítico y la planificación. Estos déficit sociales también se extienden hasta la adolescencia y la edad adulta.
Otra fuerte correlación entre las observaciones en seres humanos expuestos al cannabis durante la gestación y los modelos animales es la propensión al abuso de drogas. Como anteriormente, a diferencia de la investigación en seres humanos, los circuitos cerebrales específicos y los mecanismos moleculares subyacentes a estos cambios se han descubierto en modelos animales. Cuando las ratas están expuestas al cannabis prenatal, es más probable que desarrollen una rápida adicción a los opioides como la morfina16, especialmente si están expuestas a otras circunstancias estresantes. Esto probablemente se deba a cambios en los receptores de opioides y dopamina del cerebro que resultan de esta exposición al cannabis. Dada la actual epidemia de opioides en Estados Unidos, estos hallazgos pintan un panorama sombrío para los niños expuestos al cannabis durante el embarazo. Estos descendientes de ratones expuestos al cannabis también son más sensibles a otras drogas, como el cannabis en sí, más adelante en sus vidas. Debido a que los roedores no están sujetos a las influencias de otros factores, como el estado socioeconómico, el cuidado materno cuestionable o las influencias ambientales que pueden llevar a los seres humanos al abuso de drogas, los hallazgos en los roedores apuntan a cambios muy fundamentales en los sistemas de recompensa del cerebro que causan un aumento en la propensión al abuso de drogas y la adicción. En combinación con este tipo de otros factores, que pueden exacerbar estos cambios biológicos en seres humanos, el riesgo de abuso de drogas más adelante en la vida en seres humanos expuestos al cannabis durante el embarazo puede ser más significativo que el observado en roedores.
Finalmente, aunque hasta ahora pocos estudios han investigado los efectos de la exposición al cannabis a través de la leche materna, los datos que hasta ahora se han publicado muestran una imagen similar a la observada con la exposición durante el embarazo. Brevemente, se sabe que los cannabinoides como el THC y el CBD se transfieren de manera efectiva a través de la leche materna y llegan a los cerebros y cuerpos de la descendencia que consume leche. Debido a que estos cannabinoides son altamente lipofílicos (lo que significa que se disuelven bien en grasas) y la leche es un líquido a base de lípidos, las concentraciones de THC y CBD en la leche materna pueden ser más altas que las observadas en la sangre de la madre que consume la droga.
Nuestro laboratorio ha investigado esto tratando ratas lactantes con cannabinoides durante los primeros 10 días de vida posnatal, cuando las crías de ratas se alimentan exclusivamente de leche materna. Hemos demostrado que esta exposición a los cannabinoides a través de la leche materna causa retrasos significativos en el desarrollo del cerebro en regiones tan cruciales como la corteza prefrontal17, un centro de actividad en el cerebro que es responsable de funciones tan importantes como la planificación, el pensamiento crítico y otros llamados "funciones ejecutivas". Descubrimos que esta maduración tardía de la corteza prefrontal también se correlaciona con el desarrollo retardado de la comunicación social en estos roedores jóvenes. Nuestra investigación en curso está investigando las consecuencias a largo plazo de estos cambios, que hasta ahora parecen persistir en la edad adulta. Por lo tanto, al igual que la exposición al cannabis durante el embarazo, es probable que el consumo de cannabis durante la lactancia provoque cambios significativos y duraderos en el cerebro de la descendencia alimentada con leche materna.
Conclusiones
En conjunto, los hallazgos en los estudios epidemiológicos en seres humanos y en modelos en laboratorio de la exposición al cannabis durante el embarazo y la lactancia ponen de relieve una serie de consecuencias importantes y duraderas. Incluso dentro del útero, la conectividad de la región cerebral puede verse alterada en el feto en desarrollo por la exposición al cannabis. Si bien las deformidades físicas no se encuentran en la descendencia de madres consumidoras de cannabis, el peso bajo al nacer es más común que entre la población en general. Durante el desarrollo temprano, los niños expuestos al cannabis exhiben déficit en el aprendizaje y el comportamiento social, y son más propensos a experimentar trastornos depresivos y similares a la ansiedad, que también se correlacionan con una mayor "actuación", también conocida como comportamiento externo o agresión. Estos déficit en el aprendizaje y el comportamiento social continúan durante la adolescencia, donde los niños expuestos al cannabis también tienen más probabilidades de iniciarse en el consumo de drogas adictivas y recreativas, como el tabaco, el cannabis e incluso opiáceos como la morfina. Finalmente, aunque los datos actuales son escasos, parece que este conjunto de déficit persiste hasta la edad adulta, donde los descendientes adultos de madres consumidoras de cannabis tienen más probabilidades de experimentar dificultades cognitivas, disfunción social y una mayor propensión al abuso de drogas.
A fecha de hoy, no se conocen estrategias o curas para mejorar estos síntomas duraderos en la descendencia expuesta al cannabis. Si bien las llamadas "estrategias de rescate" se han demostrado en algunos modelos de laboratorio, siguen siendo teóricas y distantes de la aplicación pública. La única forma segura de prevenir estos problemas es no consumir cannabis o productos que contengan cannabis durante el embarazo o la lactancia. Por lo tanto, si bien el consumo de cannabis en la población general puede ser cada vez más aceptado y considerado de bajo riesgo o no conlleva un riesgo significativo, se debe evitar el uso de cannabis por parte de mujeres embarazadas y lactantes. Los obstetras y ginecólogos, así como los representantes de la industria para la venta y distribución de cannabis, deben reconocer estos peligros y trabajar para garantizar que el acceso al cannabis esté unido a un acceso equivalente a la educación.
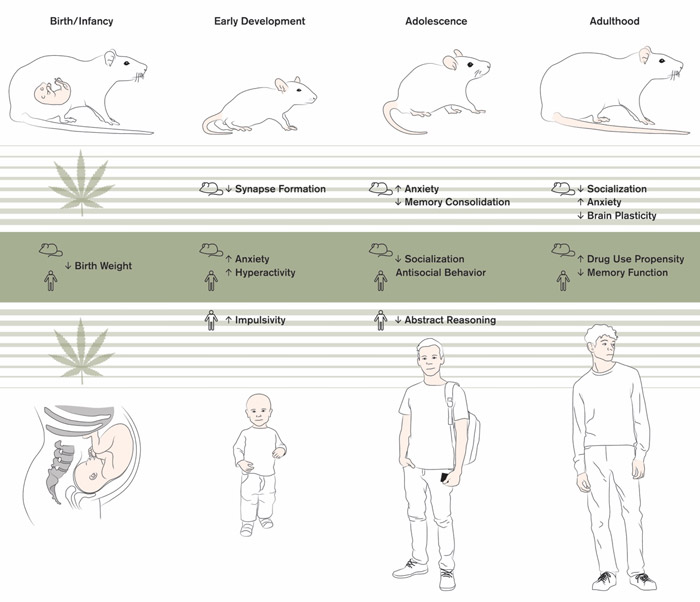
Figura 1. Resultados de por vida después de la exposición al cannabis durante el embarazo. De izquierda a derecha, las medidas de resultados selectivos desde el nacimiento hasta la edad adulta en estudios con roedores (arriba), estudios en seres humanos (abajo) y hallazgos que se han reproducido tanto en seres humanos como en roedores (centro). Adaptado de Laura F Scheyer, Trends in Neurosciences, Scheyer et al., 2019.
Referencias
1. Ko, J. Y., Farr, S. L., Tong, V. T., Creanga, A. A., & Callaghan, W. M. (2015). Prevalence and patterns of marijuana use among pregnant and nonpregnant women of reproductive age. American Journal of Obstetrics and Gynecology, 213(2), 201.e1-201.e10.
2. Dickson, B., Mansfield, C., Guiahi, M., Allshouse, A. A., Borgelt, L. M., Sheeder, J., ... Metz, T. D. (2018). Recommendations From Cannabis Dispensaries About First-Trimester Cannabis Use. Obstetrics and Gynecology, 131(6), 1031–1038.
3. Fried, P.A. and Watkinson, B. (2000) Visuoperceptual functioning differs in 9- to 12-year olds prenatally exposed to cigarettes and marihuana. Neurotoxicol. Teratol. 22, 11–20 70.
4. Fried, P.A. et al. (1992) A follow-up study of attentional behavior in 6-year-old children exposed prenatally to marihuana, cigarettes, and alcohol. Neurotoxicol. Teratol. 14, 299–311.
5. Fried, P.A. (2002) Adolescents prenatally exposed to marijuana: examination of facets of complex behaviors and comparisons with the influence of in utero cigarettes. J. Clin. Pharmacol. 42, 97S–102S.
6. Fried, P.A. et al. (2003) Differential effects on cognitive functioning in 13- to 16-year-olds prenatally exposed to cigarettes and marihuana. Neurotoxicol. Teratol. 25, 427–436.
7. Day, N. et al. (1992) The effects of prenatal tobacco and marijuana use on offspring growth from birth through 3 years of age. Neurotoxicol. Teratol. 14, 407–414.
8. Day, N.L. et al. (1994) Effect of prenatal marijuana exposure on the cognitive development of offspring at age three. Neurotoxicol. Teratol. 16, 169–175.
9. Goldschmidt, L. et al. (2000) Effects of prenatal marijuana exposure on child behavior problems at age 10. Neurotoxicol. Teratol. 22, 325–336.
10. Goldschmidt, L. et al. (2004) Prenatal marijuana and alcohol exposure and academic achievement at age 10. Neurotoxicol. Teratol. 26, 521–532.
11. Goldschmidt, L. et al. (2008) Prenatal marijuana exposure and intelligence test performance at age 6. J. Am. Acad. Child Adolesc. Psychiatry 47, 254–263. Goldschmidt, L. et al. (2012) School achievement in 14-year-old youths prenatally exposed to marijuana. Neurotoxicol. Teratol. 34, 161–167.
12. El Marroun, H. et al. (2008) Demographic, emotional and social determinants of cannabis use in early pregnancy: the Generation R study. Drug Alcohol Depend. 98, 218–226.
13. Hofman, A. et al. (2004) Growth, development and health from early fetal life until young adulthood: the Generation R Study. Paediatr. Perinat. Epidemiol. 18, 61–72.
14. Trezza, V. et al. (2012) Altering endocannabinoid neurotransmission at critical developmental ages: impact on rodent emotionality and cognitive performance. Front. Behav. Neurosci. 6, 2.
15. Antonelli, T. et al. (2005) Prenatal exposure to the CB1 receptor agonist WIN 55,212-2 causes learning disruption associated with impaired cortical NMDA receptor function and emotional reactivity changes in rat offspring. Cereb. Cortex 15, 2013–2020.
16. Vela, G. et al. (1998) Maternal exposure to delta9-tetrahydrocannabinol facilitates morphine self-administration behavior and changes regional binding to central mu opioid receptors in adult offspring female rats. Brain Res. 807, 101–109.
17. Scheyer, A.F. et al., Cannabinoid exposure via lactation in rats disrupts perinatal programming of the GABA trajectory and select early-life behaviors. Biol. Psychiatry Published online September 5, 2019.


