Door Tanja Bagar

Dr. Tanja Bagar is een microbioloog met een doctoraat in de biogeneeskunde. Ze heeft uitgebreide onderzoekservaring opgedaan in de biotechnologie, moleculaire biologie en celsignalering in laboratoria in Slovenië, Duitsland en het VK. Ze heeft zich met name gericht op het endocannabinoïde systeem en de actieve stoffen uit cannabis/hennep. Haar werk leidde tot de oprichting van het Internationale Instituut voor Cannabinoïden (ICANNA), waar ze de CEO is en voorzitter van de Expert Council. Ze is ook adjunct-directeur en hoofd R&D bij een milieubedrijf. Ze is ook actief op academisch gebied. Ze doceert microbiologie en is de decaan van de masteropleiding Ecoremediaties aan de faculteit Alma Mater Europaea.
ECS en metabolisme
Naarmate we meer leren over het endocannabinoïde systeem wordt het steeds duidelijker dat de nauwe definitie van dit systeem niet langer van toepassing is en ook geen nauwkeurige beschrijving geeft van de complexiteit van dit regulerende systeem. We weten dat ons lichaam veel endocannabinoïden produceert, dat we meer dan twee cannabinoïde receptoren hebben en dat fytocannabinoïden, of plantaardige cannabinoïden, veel moleculaire doelwitten in onze cellen en weefsels hebben. Als gevolg hiervan gebruiken sommige onderzoekers en auteurs nu een bredere definitie van het endocannabinoïde systeem, zoals het 'vergrote of uitgebreide endocannabinoïde systeem' of eenvoudigweg: het endocannabinoïdoom. Deze term omvat het geheel van endocannabinoïden, endocannabinoïde-achtige mediatoren en de vele receptoren en metabole enzymen.
Het endocannabinoïdoom speelt een zeer complexe rol bij het beheersen van veel processen in ons lichaam. Het beïnvloedt de meeste systemen in ons lichaam en de cannabinoïde receptoren komen voor in de meeste celtypen (in verschillende dichtheden). Aangezien het de biochemie reguleert van de overgrote meerderheid van de 37 biljoen cellen in ons lichaam is het niet eenvoudig om te beschrijven wat het precies doet. Onderzoek heeft aangetoond dat het endocannabinoïde systeem werkt als een soort alarmmechanisme dat wordt geactiveerd wanneer ons lichaam om de een of andere reden uit balans is. Het wordt bijvoorbeeld geactiveerd wanneer we lichamelijk letsel oplopen, bij waarneming van pathologische microben en ook wanneer we emotionele pijn voelen of stress ervaren. Het ECS lijkt te fungeren als een algemeen beschermingsmechanisme, dat begint op cellulair niveau en zich uitbreidt naar de weefsels, organen, het lichaam en ons algemeen welzijn.
Het zal geen verrassing zijn dat het endocannabinoïdoom betrokken is bij alle aspecten van ons metabolisme, waaronder onze eetlust, de energiebalans, stofwisseling, thermogenese, ontstekingen, nociceptieve pijn en de regulering van stress, beloning en emoties. Gezien de voortdurende toename van de prevalentie van stofwisselingsstoornissen, zoals obesitas, zoeken wetenschappers naar nieuwe therapeutische strategieën, waaronder het uitgebreide ECS. De componenten van het endocannabinoïdoom komen naar boven als krachtige therapeutische doelen vanwege hun rol bij het reguleren van de voedselinname en energiebalans, evenals bij de stofwisseling van lipiden en glucose. Onderzoeken hebben de upregulatie van het ECS aangetoond bij obesitas en bijbehorende stofwisselingsstoornissen. Personen met overgewicht hebben hogere concentraties endocannabinoïden dan magere personen. De verhoogde concentratie van endocannabinoïden is aangetoond in het centrale zenuwstelsel, vetweefsel, pancreas, skeletspieren, nieren, lever en bloed van knaagdieren en mensen met overgewicht. Hoewel de oorzaak nog niet helemaal duidelijk is, kan het veroorzaakt worden door een verbeterde synthese van endocannabinoïden of hun verminderde afbraak, evenals de overexpressie van cannabinoïde receptoren. Verschillende onderzoeken hebben de upregulatie van 2-AG-niveaus aangetoond in verschillende organen en serum bij obesitas en hyperglykemie, gecorreleerd aan het lichaamsvetgehalte, de viscerale vetmassa en nuchtere plasmatriacylglyceride- en insulineconcentraties. Verschillende onderzoeken hebben ook een substantieel verband aangetoond tussen het AEA-niveau en de waarde van de body mass index (BMI).
De activering van de CB1-receptor speelt een rol in het reguleren van het lipide- en glucosemetabolisme. Hoewel CB1 voornamelijk tot expressie wordt gebracht in het zenuwstelsel en de expressieniveaus in de perifere cellen laag zijn, is er een toename bij obesitas. De blokkade van CB1 vermindert de voedselinname en het lichaamsgewicht. Dit was de onderliggende gedachte voor de ontwikkeling van Rimonabant, een CB1-antagonist, die ook wordt voorgeschreven als middel tegen obesitas. Het middel had echter ernstige bijwerkingen, waaronder depressie, angst, misselijkheid, duizeligheid en zelfmoordneigingen, waarschijnlijk veroorzaakt door de blokkade van de centrale CB1. Er is aanzienlijk bewijs voor de negatieve impact van CB1 op thermogenese (warmtegeneratie van het lichaam). Onderzoekers hebben waargenomen dat muizen zonder CB1 minder vet hebben en beter beschermd zijn tegen obesitas dan vergelijkbare wilde muizen. De CB1-receptor staat bekend om zijn eetlustopwekkende effecten door de binding van THC aan deze receptoren, wat de zogenaamde munchies (vreetkick) veroorzaakt. Het effect van cannabis op het verhogen van de eetlust is al heel lang bekend. Historische bronnen geven aan dat mensen al in 300 v.Chr. wisten dat cannabis de eetlust stimuleerde, vooral de zoete en hartige trek. CB2 speelt ook een rol bij de voeding; met name de CB2-agonisten kunnen de voedselinname verminderen.
Vetweefsel
Stofwisselingsstoornissen, waaronder insulineresistentie en obesitas, zijn wereldwijd steeds vaker de voornaamste gezondheidsproblemen. Deze aandoeningen worden gekenmerkt door overmatige of abnormale vetophoping, het zogenaamde vetweefsel, en vormen belangrijke risicofactoren voor een aantal chronische ziekten, zoals hart- en vaatziekten, diabetes en in het algemeen een slechtere levenskwaliteit.
Vetweefsel onderscheidt zich gewoonlijk op basis van de kleur in wit en bruin vetweefsel. Bruin vetweefsel (BBT) wordt gekenmerkt door kleine lipide druppels en een hoge dichtheid van mitochondriën, wat de donkerbruine kleur veroorzaakt. Witte vetweefselcellen (WAT) hebben meestal maar één lipide druppel. De morfologische verschillen weerspiegelen ook verschillende functies. BBT is betrokken bij thermogenese en calorieverbruik tijdens rust en inspanning. WAT speelt een rol in de vetopslag en endocriene hormoonafscheiding. Als reactie op verschillende stimuli kan wit vetweefsel kenmerken van bruine vetcellen gaan vertonen, die beige of brite adipocyten worden genoemd.
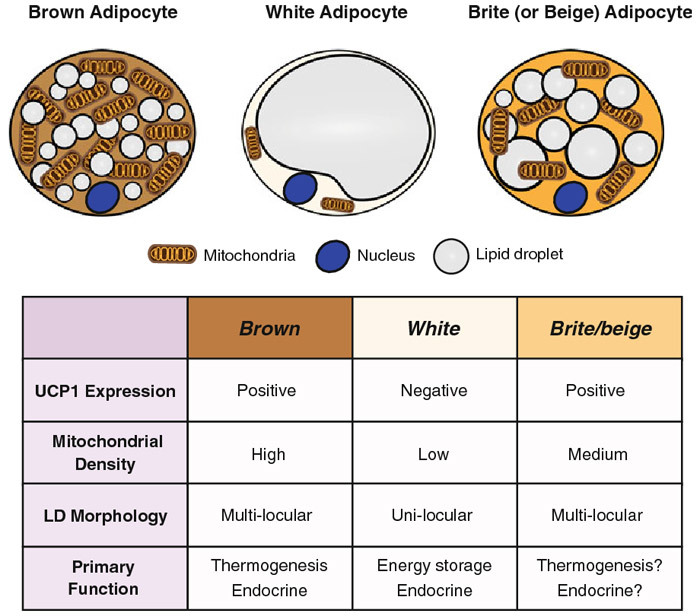
Fotobron: Jung et al., 2019
| Bruine vetcel | Witte vetcel | Brite (of beige) vetcel |
| (Mitochondria) | Kern | Lipidedruppel |
| Bruin | Wit | Brite/beige | |
| UCP1-expressie | Positief | Négative | Positive |
| Mitochondriële densiteit | Hoog | Faible | Moyenne |
| Lipidedruppel morfologie | Meerdere lipidedruppels | Uniloculaire | Multiloculaire |
| Primaire functie | Thermogenese
Endocrien |
Energieopslag
Endocrien |
Thermogenese?
Endocrien? |
Steeds meer onderzoek toont aan dat inductie of de werving van beige of brite adipocyten, samen met de activering van BBT, bescherming kunnen bieden tegen obesitas. BBT-activiteit heeft het potentieel om het lichaamsgewicht, het glucose- en lipidenmetabolisme aanzienlijk te beïnvloeden. Het speelt een rol bij het afvoeren van energie als warmte, dankzij een speciaal eiwit, UCP1 genaamd, dat voorkomt op de binnenwand van het mitochondriale membraan.
Bruine adipocyten lijken verantwoordelijk te zijn voor een grote warmteproductie, aanzienlijk hoger dan in andere organen, waardoor het energieverbruik van het lichaam wordt verhoogd. Verschillende factoren zijn in verband gebracht met het bruin worden van de WAT-vetcellen, zoals blootstelling aan kou, lichaamsbeweging, schildklierhormonen, catecholamines, capsaïcine, enz. De omzetting van WAT in beige vetweefsel is een potentieel nieuw therapeutisch doelwit voor obesitas.
Vetweefsel brengt beide cannabinoïde receptoren tot expressie en hun activering heeft een aanzienlijke invloed op de metabole activiteit van vetcellen. Men heeft aangetoond dat de blokkade van de CB1-receptor de differentiatie van witte adipocyten naar een thermogeen bruincelfenotype induceerde, wat zeer gunstig is als we vetweefsel willen verminderen. De effecten van de CB2-receptor op obesitas zijn slecht in kaart gebracht, maar we weten wel dat het sterk betrokken is bij energiehomeostase. Er is aangetoond dat de activering van CB2 de warmteontwikkeling induceert, wat energieverbruik in vetweefsel veroorzaakt. De chronische stimulatie van CB2 vermindert de toename van het lichaamsgewicht. Daarom lijkt CB2 een veelbelovend doelwit bij obesitas; het zou de anti-obesitas-effecten moeten bevorderen zonder een centrale psychotrope activiteit.
Tetrahydrocannabinol (THC)
THC is een gedeeltelijke agonist van zowel CB1- als CB2-receptoren en is het psychoactieve bestanddeel van cannabis, vanwege de binding aan de CB1-receptor in de hersenen. Bovendien activeert THC de CB1-receptoren, die zich in de limbische (verbetert de motiverende eigenschappen van voedsel) en hypothalamische (verhoogt de eetlust) regio van de hersenen bevinden, wat acute eetluststimulering of zogenaamde orexigene effecten veroorzaakt. Aan de andere kant bleek het een potentieel anti-obesitas effect te hebben. Onderzoekers hebben bij een in vivo model aangetoond dat de chronische toediening van THC aan muizen met dieet-geïnduceerde obesitas (DIO) gedurende een behandeling van 3 en 4 weken gewichtstoename voorkwam door een verminderde energie-inname. Er is ook gemeld dat THC een gunstig effect heeft op de regulatie van de insulinegevoeligheid in insulineresistente adipocyten. De mechanismen of deze dubbele effecten zijn niet volledig duidelijk, maar aangezien THC geen maximale stimulatie van CB1-receptoren produceert, zou een verklaring kunnen zijn dat de waargenomen anti-obesitas-effecten het gevolg kunnen zijn van het blokkeren van de volledige agonist, anandamide, van binding aan de CB1-receptor, met name omdat bij obesitas de endocannabinoïde toon hoog is. De mogelijke positieve invloed van THC op de preventie en de behandeling van obesitas vereist echter verder onderzoek.
Tetrahydrocannabivarine (THCV)
THCV bindt zich aan zowel cannabinoïde CB1- als CB2-receptoren. De werking lijkt dosisafhankelijk te zijn, aangezien THCV bij lage doseringen een neutrale antagonist is en een agonist bij hoge doseringen CB1- en CB2-receptoren. Omdat het een CB1-antagonistische werking heeft, leek het een veelbelovende kandidaat voor toepassing bij stofwisselingsstoornissen en obesitas. Onderzoek heeft dit gedeeltelijk bevestigd, aangezien is aangetoond dat THCV een potentieel therapeutisch effect heeft bij de behandeling van diabetes die gepaard gaat met obesitas. THCV verhoogde de insulinegevoeligheid en verbeterde de glucosetolerantie bij door voeding veroorzaakte obesitas in zowel muizen als genetisch zwaarlijvige muizen. THCV herstelde ook de intracellulaire insulinesignaleringsroute en verminderde de ophoping van lipiden in de lever en vetcellen of adipocyten. Een pilotonderzoek bij patiënten met diabetes type 2 toonde aan dat THCV de nuchtere plasmaglucose verlaagde met parallelle verbetering van de β-celfunctie in de pancreas. Dus deze fytocannabinoïde is een sterke kandidaat in de behandeling van stofwisselingsstoornissen.
Cannabidiol (CBD)
CBD heeft een breed scala aan goed onderzochte farmacologische effecten via veel verschillende mechanismen. Het is een negatieve allosterische modulator van de CB1-receptor en blokkeert de binding van sterke agonisten zoals anandamide, wat anti-obesitas effecten veroorzaakt. Aangezien het ECS overactief is bij obesitas, is er een overloop van anandamide en 2-AG. Dit leidt tot de overactivering van de CB1-receptor. Bij de CB2-receptor kan het werken als een agonist of inverse agonist, afhankelijk van de dosis en het onderzoeksmodel. CBD heeft ook affiniteit voor verschillende andere receptoren, waaronder GPR55, α1-adrenoreceptoren, 5-HT1A (serotonine), TRPV-kanalen en PPARγ. CBD vertoont veel therapeutische eigenschappen, waaronder ontstekingsremmende, antioxiderende, antitumorale, anticonvulsieve en neuroprotectieve effecten. Hierdoor is CBD een sterke kandidaat voor gebruik als potentieel therapeutisch middel in de behandeling van diabetes en de bijkomende complicaties, obesitas, ischemie, neurodegeneratieve ziekten, evenals bij pijn en depressie. Aangezien obesitas wordt geassocieerd met chronische laaggradige ontstekingen, kan CBD een cruciale rol spelen bij het verminderen van deze ontstekingsreactie en helpen een gezondere lichaamsmassa te bereiken. In dit opzicht is CBD uitgebreid bestudeerd en inmiddels is aangetoond dat CBD het niveau van glutathion (GSH), adenosinetrifosfaat (ATP) en nicotinamide-adenine-dinucleotide (NAD) verhoogt en de intracellulaire lipolyse en mitochondriale activiteit verhoogt (36). CBD heeft veel gunstige effecten op de lever, een belangrijk orgaan in alle metabolische processen en energiebalans, omdat het leversteatose (verminderde ophoping van triacylglyceriden en lipide druppels), ontstekingsreactie en nitratieve stress vermindert, Ook vermindert het lipideperoxidatie, de expressie van reactieve zuurstofcomponenten (ROS) en infiltratie van neutrofielen in de lever. De effecten van CBD op voedselinname, voedselvoorkeuren en gewichtstoename waren onduidelijk en gaven een reeks verwarrende resultaten weer. Eén onderzoek toonde aan dat CBD een afname van de lichaamsgewichtstoename bij ratten veroorzaakte, terwijl andere onderzoeken geen significante invloed op de voedselinname en het lichaamsgewicht bij muizen en ratten hebben aangetoond. Eén onderzoek toonde ook aan dat CBD bij ratten die een vetrijk dieet kregen, leidde tot een toename van het lichaamsgewicht, ondanks een aanzienlijk verminderde voedselinname. Ongeacht de tegenstrijdige resultaten van CBD bij voeding, heeft CBD veelvoudige gunstige effecten op diverse veranderingen en pathologieën die een rol spelen bij obesitas. Omdat het zich aan veel receptoren bindt, heeft het effecten op veel organen die cruciaal zijn voor het metabolisme, zoals de lever, vetweefsel, pancreas en hart. Het is ook Interessant dat er een verschuiving plaatsvond in de relevante veranderingen in de darmhormonen, zoals de GIP-glucose-afhankelijke insulinotrope peptide- en adipokines-concentraties.
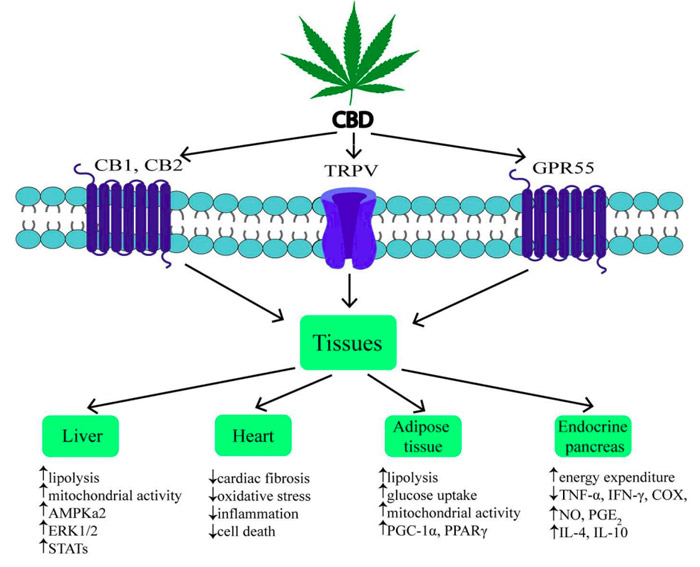
Fotobron Bielawiec et al., 2020
| CBD | |||
| CB1, CB2 | TRPV | GPR55 | |
| Weefsel (Tissues) | |||
| Lever | Hart | Vetweefsel | Endocriene pancreas |
| ↑ Vetafbraak | ↓ Hartfibrose | ↑ Vetafbraak | ↑ Energieverbruik |
| ↑ Mitochondriale activiteit | ↓ Oxidatieve stress | ↑ Toename glucose | ↓ TNF-α, IFN-γ, COX |
| ↑ AMPKa2 | ↓ Ontsteking | ↑ Mitochondriale activiteit | ↑ NO, PGE |
| ↑ ERK1/2 | ↓ Celsterfte | ↑ PGC-1α, PPARγ | ↑ IL-4, IL-10 |
| ↑ STAT | |||
Conclusie
De aan obesitas gerelateerde co-morbiditeit neemt toe. Dit leidt tot hoge kosten voor de samenleving en vermindert de levenskwaliteit van patiënten. Recente bevindingen op het gebied van het bruin worden van wit vetweefsel (de transformatie van WAT naar BBT) wijzen op de mogelijke rol van dit fenomeen bij de behandeling van obesitas. De BBT-activiteit is in verband gebracht met een verbetering van het metabool profiel bij volwassenen. De activering van CB2 verbetert de bruining en het omzetten van chemische energie in thermische energie, wat een belangrijk stukje in de puzzel zou kunnen zijn.
Het is ook belangrijk om ons te richten op CB1. Maar we mogen daarbij de ervaringen met Rimonabant niet vergeten. Deze CB1-receptorantagonist leek tijdens klinische onderzoeken een veelbelovend geneesmiddel tegen obesitas te zijn, maar vertoonde ook enorme psychiatrische bijwerkingen en moest uit de handel worden genomen. De stopzetting van klinische proeven met de FAAH-remmer vanwege het optreden van ernstige bijwerkingen heeft ook aangetoond dat het beïnvloeden van dit essentiële fundamentele beschermingssysteem heel zorgvuldig moet worden gedaan. Ook hier vertonen fytocannabinoïden, naast andere liganden, veel potentieel. De focus ligt op het vinden van plantaardige CB1-receptorantagonisten en CB2-receptoragonisten. Deze vertonen een hoog veiligheidsprofiel met verwaarloosbare bijwerkingen en hebben meerdere doelen binnen het endocannabinoïdoom die een gezond metabolisme, energieverbruik, biochemische homeostase en emotioneel welzijn ondersteunen.
Literatuurbronnen
Jung SM, Sanchez-Gurmaches J, Guertin DA. Brown Adipose Tissue Development and Metabolism. Handb Exp Pharmacol. 2019;251:3-36. doi: 10.1007/164_2018_168. PMID: 30203328; PMCID: PMC7330484.
Bielawiec P, Harasim-Symbor E, Chabowski A. Phytocannabinoids: Useful Drugs for the Treatment of Obesity? Special Focus on Cannabidiol. Front Endocrinol (Lausanne). 2020 Mar 4;11:114. doi: 10.3389/fendo.2020.00114. PMID: 32194509; PMCID: PMC7064444.
Rossi F, Punzo F, Umano GR, Argenziano M, Miraglia Del Giudice E. Role of Cannabinoids in Obesity. Int J Mol Sci. 2018 Sep 10;19(9):2690. doi: 10.3390/ijms19092690. PMID: 30201891; PMCID: PMC6163475.
Borowska M, Czarnywojtek A, Sawicka-Gutaj N, Woliński K, Płazińska MT, Mikołajczak P, Ruchała M. The effects of cannabinoids on the endocrine system. Endokrynol Pol. 2018;69(6):705-719. doi: 10.5603/EP.a2018.0072. PMID: 30618031.
Kaur R, Ambwani SR, Singh S. Endocannabinoid System: A Multi-Facet Therapeutic Target. Curr Clin Pharmacol. 2016;11(2):110-7. doi: 10.2174/1574884711666160418105339. PMID: 27086601.
Behl T, Chadha S, Sachdeva M, Sehgal A, Kumar A, Dhruv, Venkatachalam T, Hafeez A, Aleya L, Arora S, Batiha GE, Nijhawan P, Bungau S. Understanding the possible role of endocannabinoid system in obesity. Prostaglandins Other Lipid Mediat. 2021 Feb;152:106520. doi: 10.1016/j.prostaglandins.2020.106520. Epub 2020 Nov 26. PMID: 33249225.
Abioye A, Ayodele O, Marinkovic A, Patidar R, Akinwekomi A, Sanyaolu A. Δ9-Tetrahydrocannabivarin (THCV): a commentary on potential therapeutic benefit for the management of obesity and diabetes. J Cannabis Res. 2020 Jan 31;2(1):6. doi: 10.1186/s42238-020-0016-7. PMID: 33526143; PMCID: PMC7819335.