Por Ismael Galve-Roperh

Ismael Galve-Roperh, Bioquímico y biólogo molecular con más de 20 años de experiencia de investigación en cannabinoides. Ha realizado importantes contribuciones como el descubrimiento del papel antitumoral de la señalización cannabinoide, sus efectos neuroprotectores en enfermedades neurodegenerativas o el impacto en el neurodesarrollo de estos compuestos.
Ismael Galve-Roperh1, Alline Campos2, Francisco Guimaraes2, Manuel Guzmán1
1 Facultad de Biología e Instituto Universitario Investigación Neuroquímica, Universidad Complutense, 28040 Madrid (España), Centro de Investigación Biomédica en Red sobre Enfermedades Neurodegenerativas (CIBERNED) Instituto Ramón y Cajal de Investigaciones Sanitarias (IRYCIS);
2 Departamento de Neurofarmacología, Universidad de São Paulo, Riberao preto, Brasil
Recientemente, se ha puesto en marcha la primera red de investigación sobre cannabinoides de América Latina financiada con fondos públicos (CannaLatan, www.cyted.org/es/cannalatan), formada por investigadores universitarios y empresas farmacéuticas de diferentes países. CannaLatan tiene como objetivo promover y potenciar los resultados obtenidos por los diferentes miembros del consorcio desarrollando, en colaboración, proyectos de investigación y educación. La red CannaLatan se dedica a estudiar las posibles aplicaciones terapéuticas de fitocannabinoides poco investigados y de nuevas moléculas basadas en cannabinoides, así como a clarificar sus efectos no deseados. Aquí hablamos de uno de los proyectos en curso iniciado por CannaLatan con el apoyo financiero de la Fundación Canna (www.fundacion-canna.es/), en el que abordamos los efectos antipsicóticos y cognitivos de las formas ácidas de los fitocannabinoides, en concreto el THCa (Figura 1A).
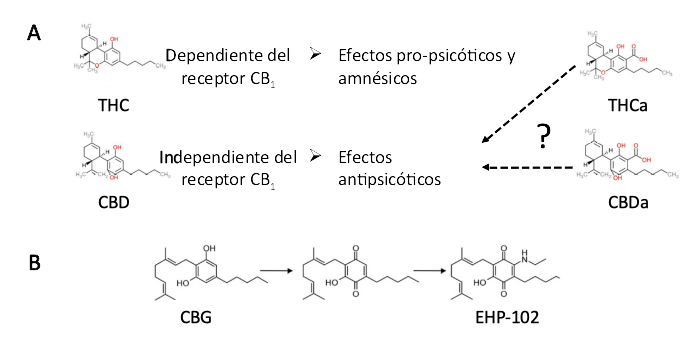
Leyenda de las figuras. A, Efectos diferenciales de las formas neutras y ácidas de los dos fitocannabinoides más investigados, THC y CBD. B, Uso de plantillas estructurales de fitocannabinoides para el desarrollo de moléculas terapéuticas mejoradas, como se ejemplifica con los derivados de quinona CBG.
La planta Cannabis sativa contiene más de 160 moléculas con una gran diversidad de modificaciones químicas basadas en una estructura de andamiaje común (núcleo policétido de resorcinol isoprenilado) y conocidas como los fitocannabinoides (Hanuš et al., 2016). El THC (delta-9- tetrahidrocannabinol) y el CBD (cannabidiol) son, con diferencia, las moléculas que más se han investigado. El interés de la comunidad científica durante el siglo XX por el mecanismo de acción del THC ha estado impulsado sobre todo por las instituciones antidroga, que pretendían demostrar y difundir sus efectos nocivos. En este sentido, mientras que el uso del THC, como el de cualquier otra molécula bioactiva, no está exento de efectos no deseados (Ferland and Hurd, 2020), los científicos han ido aceptando e investigando poco a poco la gran variedad de posibles aplicaciones beneficiosas del THC conocidas por la humanidad desde hace milenios. El THC es una molécula psicoactiva que regula la función neuronal principalmente a través de los receptores cannabinoides CB1, que fueron identificados y clonados en la década de los noventa. De manera distinta, el interés por el CBD es mucho más reciente. El CBD ha sido ignorado por los científicos como una molécula «no activa», siendo una de las principales razones de esta falta de interés, la ausencia de un mecanismo de acción mediado por el receptor. Curiosamente, el CBD ha pasado en los últimos tiempos del ostracismo a ser la molécula cannabinoide preferida, ya que i) es un compuesto no psicotomimético (no induce psicosis, característica de las moléculas dirigidas al receptor CB1 como el THC; ii) el CBD ejerce efectos anticonvulsivantes en diversas enfermedades epilépticas refractarias, lo que ha llevado a la FDA y a la EMA a aprobar su uso como medicamento; y iii) la ausencia de efectos pro-psicóticos y de deterioro cognitivo del CBD lo libra de la mayoría de las restricciones de acceso que se aplican al THC. Por lo tanto, el CBD es un compuesto seguro y muy bien tolerado que ha explotado como la molécula «de oro» del Cannabis y se ha convertido en el compuesto preferido para el marketing comercial, añadiéndose ahora a muchos productos de consumo humano y comestibles (productos presentados como beneficiosos para la salud, suplementos nutricionales y cualquier otra cosa que se pueda imaginar). La eficacia de la mayoría de los productos que contienen CBD, no de pureza farmacéutica, con concentraciones bajas o indeterminadas de CBD, ausencia de biodisponibilidad y datos farmacodinámicos puede ser cuestionada en muchos casos. Sin embargo, el CBD es una molécula interesante por sus supuestos usos terapéuticos. Entre otras propiedades terapéuticas (Fernández-Ruiz et al., 2020), el CBD ejerce un efecto anticonvulsivante en la epilepsia y alivia los síntomas de varios trastornos neuropsiquiátricos. En este sentido, se ha demostrado repetidamente que el CBD ejerce efectos ansiolíticos, antidepresivos y antipsicóticos en modelos preclínicos de diversos estados patológicos (Figura 1A). Existen pruebas razonables de que el CBD alivia los síntomas de la esquizofrenia, el trastorno de ansiedad social, las comorbilidades del trastorno del espectro autista y el trastorno por déficit de atención e hiperactividad en humanos (Crippa et al., 2020). Por último, pero no por ello menos importante, se está explorando el CBD para el tratamiento de los síntomas no motores de las enfermedades neurodegenerativas (es decir, la enfermedad de Parkinson y la enfermedad de Alzheimer), por mencionar algunos ejemplos.
Además de la modulación aguda de los aspectos conductuales, los cannabinoides también pueden influir en el destino de las células neuronales, controlando las vías de señalización de supervivencia y muerte celular. El THC puede ejercer efectos a favor de la supervivencia de las neuronas en las enfermedades neurodegenerativas y contrarrestar la muerte de las células inducida por insultos neuronales agudos (excitotoxicidad, daño hipóxico-isquémico, lesión cerebral traumática y otros)(Di Marzo et al., 2015). Resulta interesante que el THC, al actuar sobre los receptores CB1 localizados en las células progenitoras neuronales, y el CBD, al actuar a través de mecanismos aún poco claros, promuevan la generación de neuronas recién nacidas en el cerebro del ratón adulto (Diaz-Alonso et al., 2012). Este proceso, conocido como «neurogénesis adulta», tiene lugar en áreas cerebrales diferenciadas (hipocampo y zona subventricular) de los roedores, y su existencia y relevancia en el cerebro humano es objeto de controversia y debate. En general, el «dúo» THC-CBD ejerce efectos beneficiosos complementarios en los estados patológicos del sistema nervioso. Sin embargo, el mecanismo de acción del CBD sigue siendo poco claro, aunque se ha demostrado que modula varios receptores y vías de señalización. En cualquier caso, es importante tener en cuenta que, al menos hasta la fecha, la mayoría de los efectos terapéuticos demostrados de los productos basados en cannabinoides se deben posiblemente a su contenido de THC (www.fundacion-canna.es/cannabis-vs-thc-son-realmente-tan-distintos).
Además del THC y el CBD, una nueva corriente/tendencia de investigación pretende abordar el impacto fisiológico de otros cannabinoides menores presentes en la planta [es decir, el THCa (ácido tetrahidrocannabinólico), el CBDa (ácido cannabidiólico), el ácido cannabigerólico (CBGa), la tetrahidrocannabivarina (THCV), la cannabidivarina (CBDV), el cannabicromeno (CBC) y su forma ácida CBCa y otros](Stone et al., 2020). Los fitocannabinoides se producen mediante complejas vías metabólicas, y el cannabigerol (CBG) se considera el precursor común de la mayoría de ellos. Normalmente, el THCa y otras formas ácidas de los cannabinoides se convierten en sus formas moleculares bioactivas neutras mediante la descarboxilación inducida por el calor. Se está intentando dilucidar si estas formas ácidas de los cannabinoides podrían ser de interés terapéutico, ya que hasta ahora se consideran desprovistas de efectos psicoactivos no deseados. Nuevos datos recientes sugieren que el CBG, el CBDV y el THCV, así como el THCa y el CBDa, podrían ser útiles para tratar algunos síntomas de enfermedades neurológicas y psiquiátricas (Figura 1A). Aunque las pruebas disponibles son todavía débiles y requieren más investigación, el THCa es neuroprotector en ratones al actuar a través de los receptores nucleares PPARγ y se ha sugerido que ejerce efectos inmunomoduladores. También atenúa la adiposidad y las enfermedades metabólicas causadas por la obesidad inducida por la dieta.
Utilizando el modelo preclínico del antagonismo del receptor de glutamato NMDA, los grupos de la Universidad de São Paulo (Brasil) y de la Universidad Complutense (España) están evaluando los supuestos efectos antipsicóticos y ansiolíticos del THCa. La administración de THCa a roedores rescató los déficits de interacción social y función cognitiva, evaluados por la prueba de reconocimiento de objetos nuevos. Es importante destacar que el THCa fue tan eficaz como el fármaco antipsicótico típico, clozapina. Las investigaciones en curso se centran en determinar el mecanismo de acción molecular del THCa, que puede implicar la regulación de los PPARγ, o la formación de heterómeros del receptor CB1, de forma similar a otros fitocannabinoides como el CBD y el CBG. En cuanto a otros cannabinoides ácidos homólogos, el CBDa es neuroprotector, aunque actúa a través de mecanismos diferentes a los del CBD. Además, el CBDa previene la emesis y los vómitos, siendo más potente que su forma neutra de CBD. La acción antinociceptiva de los cannabinoides dirigidos al receptor CB1 también se observa con el CBDa. Se ha demostrado que el CBGa induce efectos anticonvulsivantes o proconvulsivantes en diferentes modelos preclínicos de epilepsia.
Desgraciadamente, el campo de las aplicaciones terapéuticas de los cannabinoides está limitado por la exigencia de fomentar los beneficios económicos para la industria que está detrás. Algunas empresas desarrollan sus estrategias de beneficio económico mediante la protección de la propiedad intelectual de los métodos de administración, aislamiento y purificación de cannabinoides. Otros han optado por diseñar nuevas estructuras moleculares mediante la modificación química de los fitocannabinoides para mejorar sus efectos terapéuticos, mejorar su biodisponibilidad y atenuar sus efectos no deseados (Figura 1B). Entre otros, se han desarrollado derivados del CBD y del CBG, como los compuestos EHP-101 y EHP-102, respectivamente, lo que ha permitido identificar moléculas de interés que cumplen algunos de estos criterios. Los compuestos EHP se han investigado activamente por sus efectos terapéuticos contra las consecuencias de las enfermedades neurodegenerativas y neuroinflamatorias. La investigación preclínica logró identificar que el derivado del CBG EHP-102, al actuar a través de los PPARγ es neuroprotector en modelos de ratón de la enfermedad de Huntington. El efecto neuroprotector del EHP-102 se suma a su efecto proneurógeno, por lo que aumenta la generación de neuronas derivadas de la zona subventricular que migran hacia el estriado degenerado. Cabe destacar que esta molécula es eficaz por vía oral y, como agonista parcial del receptor, no induce los efectos perjudiciales característicos de los agonistas completos de los PPARγ . Otro fármaco prometedor, el HU-580, basado en la modificación del éster metílico del CBDa, se está investigando por sus efectos contra las náuseas y ansiolíticos.
En resumen, la investigación sobre los potenciales efectos terapéuticos de los cannabinoides ha experimentado un crecimiento exponencial en las últimas décadas y ha logrado identificar y demostrar interesantes efectos beneficiosos para el THC y el CBD. Mientras que todavía se necesita más investigación básica y sólida, y sobre todo, ensayos clínicos estandarizados para avanzar en la traslación de la investigación preclínica del laboratorio a la práctica clínica para estas moléculas, se exploran activamente nuevas vías para identificar si otros fitocannabinoides menores son de interés para fines biomédicos. Pronosticamos que, en el futuro, el campo de los cannabinoides se beneficiará de la diversidad de las moléculas derivadas de las plantas y demostrará nuevas aplicaciones para el tratamiento de los trastornos del sistema nervioso y sus síntomas.
Agradecimientos: Financiación Cyted de la red CannaLatan, Fundación Canna por su apoyo a la investigación del THCa, y Phytoplant Research (España) por la amable donación de fitocannabinoides purificados.
Referencias seleccionadas
Crippa JA, de Lima Osório F, Hallak J, Guimarães FS, Zuardi AW. Cannabinoids for the treatment of mental disorders. The Lancet Psychiatry 2020; 7: 125–126.
Diaz-Alonso J, Guzman M, Galve-Roperh I, Díaz-Alonso J, Guzmán M, Galve-Roperh I. Endocannabinoids via CB₁ receptors act as neurogenic niche cues during cortical development. Philos Trans R Soc Lond B Biol Sci 2012; 367: 3229-41.
Ferland JMN, Hurd YL. Deconstructing the neurobiology of cannabis use disorder. Nat Neurosci 2020; 23: 600-610.
Fernández-Ruiz J, Galve-Roperh I, Sagredo O, Guzmán M. Possible therapeutic applications of cannabis in the neuropsychopharmacology field. Eur Neuropsychopharmacol 2020: 1-18.
Hanuš LO, Meyer SM, Muñoz E, Taglialatela-Scafati O, Appendino G. Phytocannabinoids: A unified critical inventory. 2016
Di Marzo V, Stella N, Zimmer A. Endocannabinoid signalling and the deteriorating brain. Nat Rev Neurosci 2015; 16: 30-42.
Stone NL, Murphy AJ, England TJ, O'Sullivan SE. A systematic review of minor phytocannabinoids with promising neuroprotective potential. Br J Pharmacol 2020; 177: 4330-4352.


